Málmar eiga það sameiginlegt að hafa fáar gildisrafeindir. Alkalímálmarnir hafa aðeins eina og jarðalkalímálmarnir tvær. Þessar rafeindir eru tiltölulega lausar og slitna því auðveldlega af málmatómunum. Þegar frumeind (atóm) missir rafeind þannig að neikvæðu rafeindahleðslurnar verða færri en jákvæðu kjarnahleðslurnar myndast jákvætt hlaðin atómjón sem kallast katjón. Gott dæmi um slíkar jónir eru jónir alkalí-, jarðalkalímálmanna auk annarra málma. (Sbr. lotukerfið, ◊  ). Dæmi um málma eru natrín, magnesín, járn og ál. Jónir þeirra eru táknaðar á eftirfarandi hátt: Na+, Mg+2 og Al+3. Plúshleðslan sýnir hve margar rafeindir atómin hafa misst og í þessum tilfellum hafa allar gildisrafeindir viðkomandi atóma fallið brott.
). Dæmi um málma eru natrín, magnesín, járn og ál. Jónir þeirra eru táknaðar á eftirfarandi hátt: Na+, Mg+2 og Al+3. Plúshleðslan sýnir hve margar rafeindir atómin hafa misst og í þessum tilfellum hafa allar gildisrafeindir viðkomandi atóma fallið brott.
Önnur frumefni, einkum málmleysingjar, hafa margar gildisrafeindir og reyna því að fylla gildishvelið með því að bæta við sig rafeindum. Við það verða neikvæðu hleðslurnar fleiri en jákvæðu hleðslurnar í kjarnanum og fá þau þannig neikvæða hleðslu út á við og kallast anjónir. Dæmi um þessi frumefni eru klór, brennisteinn og súrefni (Cl-, S-2 og O-2). Þótt anjónirnar séu örsmáar eru þær mun stærri en katjónirnar. ◊ 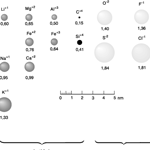
Lotukerfið 600x431px ◊  , 800x580px ◊
, 800x580px ◊ 
Til baka í gildisrafeind.